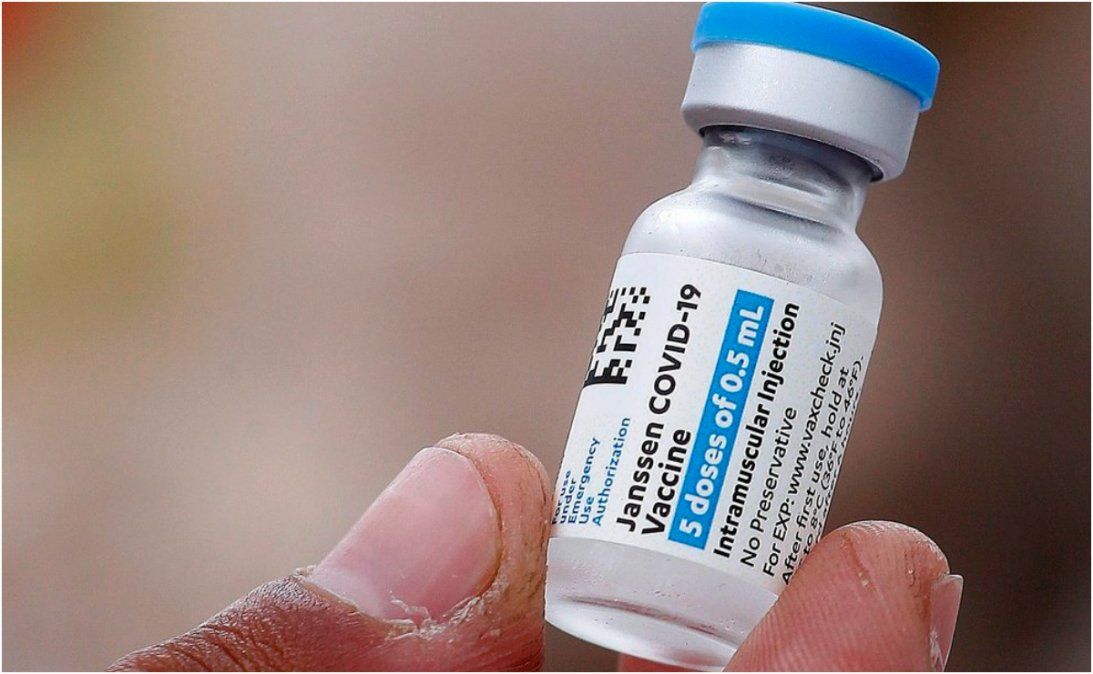
La resolución señala que se le otorga el “registro de emergencia” a la vacuna monodosis de Janssen Pharmaceuticals, conocida también como la de Johnson & Johnson.
La disposición 7502 con fecha del 1 de octubre, del organismo de control de medicamentos nacional señala: “Autorizarse a la firma Janssen Cilag Farmacéutica S.A. en el contexto de Pandemia Covid 19, la inscripción condicional a los fines de su uso en el Registro de Especialidades Medicinales (REM) y de la Administración Nacional De Medicamentos, Alimentos Y Tecnología Médica de la especialidad medicinal de nombre comercial Covid-19 Vaccine Janssen y nombre genérico Vacuna Contra Covid-19, la que de acuerdo a lo solicitado, será comercializada en la República Argentina por Janssen Cilag Farmacéutica S.A de acuerdo con los datos identificatorios característicos del producto incluidos en el Certificado de inscripción”.
En el artículo 2° se especifica que “en virtud de tratarse de una autorización condicional, la vigencia del Certificado será de 1 (UN) año a partir de la fecha de la presente Disposición”.
El documento, que lleva la firma de Manuel Limeres de la ANMAT, aclara que la empresa deberá “presentar los informes de seguridad periódicos cada 6 meses luego de la comercialización efectiva del producto ante el INAME (Instituto Nacional de Medicamentos)”.
Además especifica que “todo cambio en el perfil de seguridad o de eficacia del producto deberá evidenciarse en la correspondiente modificación del prospecto”. Y que, en el caso de incumplimiento de las obligaciones previstas, la ANMAT podrá “suspender la comercialización del producto aprobado por la presente disposición, cuando consideraciones de salud pública así lo ameriten”.